
484亿好意思元。
这是本年上半年,国产翻新药的出海交游总金额。2025年前六个月的发达已接近2024年全年水平,达到历史新高。
在中国新动力汽车和东说念主工智能等产业领域强势崛起的同期,翻新药也在成为中国在高新时候领域突破的典型代表。
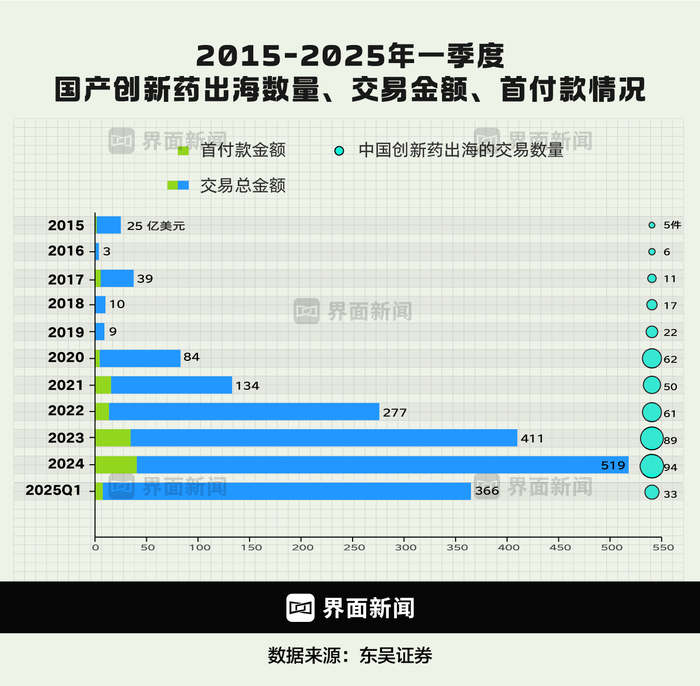 图为中国翻新药出海交游近10年的变化 制图:界面新闻 何苗
图为中国翻新药出海交游近10年的变化 制图:界面新闻 何苗
与仿制药研发壁垒低,价值更在普惠不同,翻新药面对的永远是东说念主类人命健康中尚无解法的难题——比如癌症、凄婉病。医药行业用“十年时刻,十亿好意思元”轮廓其研发的长周期、高风险和高成本。也有东说念主将这个进程比作大把资产、筹备与分子科学混调而成的烈酒。
作念国产翻新药、以至带中国翻新药走向公共,一直是国内翻新药行业的愿景。近半年来,中国医药企业接连掀翻的巨浪正带着这些逸想冉冉走向现实。
本年5月,老牌药企三生制药以12.5亿好意思元的首付款价钱将一款在研双抗翻新药的国外权利出售给“天地大药厂”辉瑞,一举冲破了国产翻新药对外授权交游首付款的最高记载。
除三生制药外,信达生物、和铂医药等也都先后与国外大药企达成单笔交游总价超10亿好意思元的对外授权。
在融资与支付上,7月的第一周,国度医保局、国度卫健委团结印发《相沿翻新药高质地发展的多少递次》,翻新药商保目次申诉不得不发。而禾元生物IPO告捷过会则意味着,尘封已久的科创板再次对未盈利生物医药公司掀开了大门。
仿佛短短几个月内,“翻新药寒冬”毅然九霄,国产翻新药们迎来了我方的新一波海浪。
01 起初的逸想
风起于青萍之末,中国翻新药参加公众视线是在这半年,而这条路却也曾走了20多年。
2002年,瑞士巨头诺华制药的白血病药物伊马替尼(格列卫)刚刚在好意思国获批,肿瘤靶向休养期间的大幕缓缓拉开。同在这一年,李嘉诚投资的和黄医药也在上海确立,成为国内最早从事翻新药研发的公司之一。它起初的职工包括自后的再鼎医药创举东说念主杜莹、亚虹医药创举东说念主潘柯。
一年后,留好意思的丁列明与玉玺祥归国创立贝达药业,研发埃克替尼,也就是日后中国的首款国产小分子抗癌药。2009年,曾任好意思国密歇根大学副提拔的杨大俊在上海创办了亚盛医药。
这批最早的海归见证过好意思国安靖的翻新药行业奈何一步步发展壮大。但想把大洋此岸的盛景移植过来绝非易事。彼时国内翻新药研发领域则号称盐碱地。由于新药界说宽松,审评尺度又不透明,递往药监局的各式审批贵府严重积压,很多公司在递交申诉材料之后就堕入无限的恭候。
恶浊初开时期的首要不细目性,让风险投资都对国产翻新药避之不足。贝达药业创举东说念主丁列明曾回忆,研发埃克替尼时,他一度找不到钱作念该药的III期临床筹商。
变化始于2015年,彼时的原国度食药监局开启了国内一系列药审改良。翻新药尺度启动与国际对都,饱读吹新药研发、加快新药审批上市。
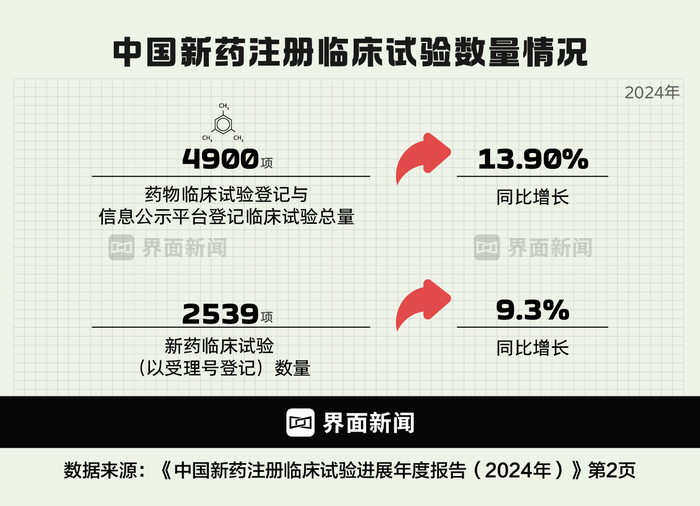 图为中国翻新药临床开展情况的近些年变化 制图:界面新闻 何苗
图为中国翻新药临床开展情况的近些年变化 制图:界面新闻 何苗
如百济神州,亚盛医药等最早破土而出的创业公司渐渐走上台前。
另一方面,其时的国度食药监局也入辖下手鼓励仿制药一致性评价,为日后的带量采购、控费作念好铺垫。带量采购的出现意味着仿制药的利润例必将薄如刀片,也加快了传统安靖药企向研发翻新药转型。
以仿制药起家的恒瑞医药在2018年文告,只作念翻新药和有中枢价值的高端仿制药。
成本市集也在发力,2018年的“港股18A”、2019年的科创板新规,允许未盈利的生物科技公司上市,都给刚踉跄起步的国内翻新药公司径直插上了翅膀。
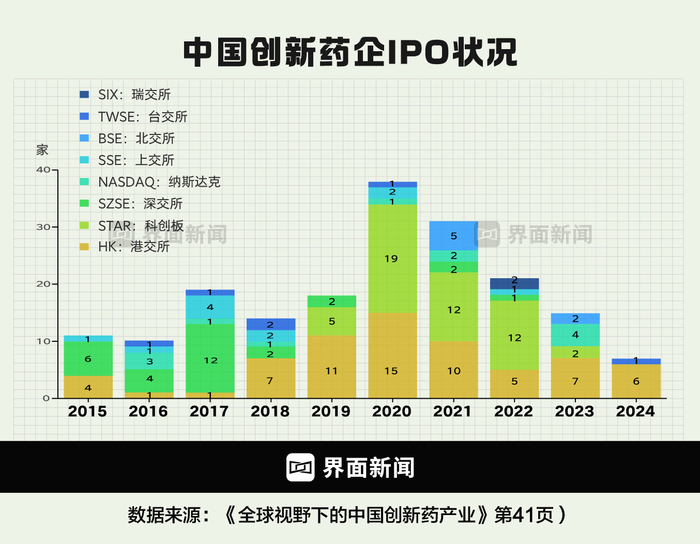 图为中国翻新药企业IPO情况 制图:界面新闻 何苗
图为中国翻新药企业IPO情况 制图:界面新闻 何苗
阅历光鲜的创举团队加上漂亮的管线图就能引来投资,开启天神轮和风投并同步递交招股书仿佛也并非痴东说念主说梦,大宗一线有名翻新药企都在这几年里实现了IPO。
中国翻新药就在这么得意、热辣的敌视下,迎来了第一波海浪。
02 研发求变
然而这股海浪并莫得抓续太久。
其时,中国的翻新药公司在立项开发上多领受随从策略,紧盯国外翻新药的研发进展,跟在后头作念同类居品。
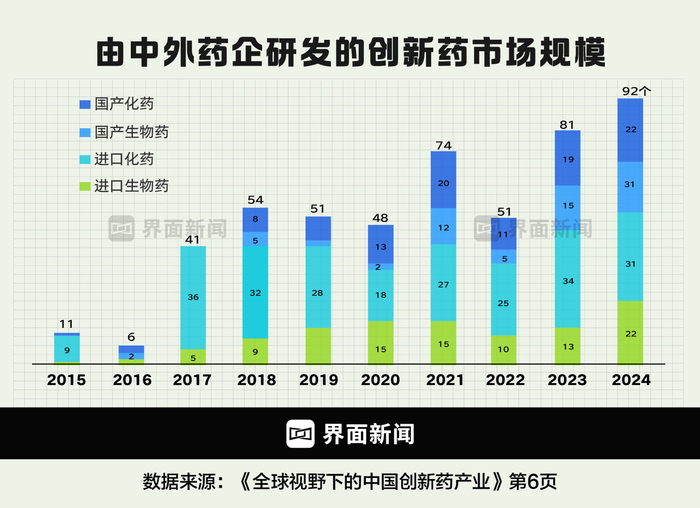 图为近些年国产和入口翻新药获批数目 制图:界面新闻 何苗
图为近些年国产和入口翻新药获批数目 制图:界面新闻 何苗
2014年,默沙东帕博利珠单抗在好意思国获批,这款俗称K药的PD-1单抗成为癌症休养史上的里程碑式药物,并在自后以300亿好意思元的年销售额成为公共“药王”。
于是在那几年,国内的PD-1数目多到被临床筹商者戏称“满盈用来洗沐”。到2020年,最早上市的四款国产PD-1以降价60%-80%的代价参加国度医保目次。同质化也导致“价钱战”硝烟四起。
短短两年时刻,千亿级国内PD-1市集缩水三分之二,只剩下两三百亿。2023年7月,恒生翻新药指数跌到了历史最低点,比较于2021年7月的顶峰已下落76%,翻新药行业由盛夏疾速转入穷冬。
好在故事莫得就此末端。
研发出一款新药像是在热暑中跑超长程的马拉松。信得过以此为志的东说念主常常不乏超常的韧劲和洪志。
就像亚盛医药创举东说念主杨大俊对界面新闻说的那样,算作最早出洋、在好意思国时作念最前沿筹商、又很早归国的“凫水儿”,他归国创业时就定下了要作念原始翻新的主见。
所有这个词产业也在吸取教育、从最启动的研发端悄然起变。
2012年,夏瑜等东说念主在广东中山确立康方生物。这家公司英文名Akeso源自希腊诊疗女神。在同业不看好的眼神中,康方生物入辖下手研发兼具无为疗效又安全的PD-1双抗。2024年,其一款中枢PD-1双抗药物在严格比对中初次投降默沙东的药王K药。
在第一波海浪的淘汰赛里,那些存活况兼顺利出海的公司重塑了国内翻新药产业的发展念念路——单纯师法国外居品已不再能豪恣拉来投资,更强调速率和互异化翻新。
百济神州的泽布替尼和传奇生物的CAR-T疗法西达基奥仑赛,成为两个额外瞩目又贫瘠的例子。两者用于休养不同的血液肿瘤,先后都告捷在好意思国获批上市。更迫切的是,它们分散打败了来自国际制药巨头强生/艾伯维和百时好意思施贵宝的同类竞品,双双被诠释具有更优异的疗效和安全性,成为各自赛说念上的同类最优药物。
2023年,百济神州的泽布替尼成为首个销售额超10亿好意思元的国产抗癌药;传奇生物的西达基奥仑赛如今距“十亿好意思元分子”也只差一步之遥。
现任恒瑞医药副总裁、上海恒瑞CEO的贺峰博士向界面新闻回忆,十年前,公司研发东说念主员很少参加国际学术会议,原因很浮浅——没太多需求。而约从4、5年前起,公司启动条目要么作念同类起初(FIC,first-in-class)、要么作念同类最优(BIC,best-in-class)。恒瑞医药每年也组织起宏大的研发与商务拓展团队参与各式国际学术会议,来增进学问与信断相通,加强翻新敏锐度。
贺峰对界面新闻先容,对于同类最优名目,早研部门需要尽可能筹商绝对袪除赛说念上的竞品,能找到显然切入点的上风名目才会开题;而其他名目,“不只是早研阶段,还条目临床阶段,都要保证是公共前哨”。
03 重塑“中国信誉”
固然,同类起初和同类最优莫得一个好作念,都是难啃的硬骨头。
前者莫得前例能参考,海表里从前驱作念成先烈的公司不在少数;后者挑战的则是先驱已充分筹商但依旧无法处理的软肋。
作念翻新药的特别之处在于,制药东说念主得与难以捉摸的大当然和人命体交手。细目性只可逐渐地来自于满盈多且可靠的临床数据,并一直到空想中的新药信得过被告捷开发出来。
在苏州宜联生物创举东说念主、董事长兼CEO薛彤彤看来,如今国产翻新药变成骄子、密集出现更大额的出海授权,中国翻新药行业在往日5年里共同完成的使命即是蕴蓄临床数据和国外信誉,最终得以诠释自己价值。
 图为宜联生物研发部门 图片起首:宜联生物
图为宜联生物研发部门 图片起首:宜联生物
据摩熵医药中国临床进修数据库,2019年至2024年,中国临床进修登记总量由2385项提高至4884项,年复合增长率达15%,其中新药研发占比过半。
贺峰告诉界面新闻,在本年6月刚刚末端的好意思国临床肿瘤学会(ASCO)上,来自中国翻新药的理论讲演都占据了三分之一。
ASCO是公共界限最大、级别最高的肿瘤学术会议之一。本年,恒瑞医药以理论讲演的方式分享了一项对于乳腺癌翻新药达尔西利辅助休养的筹商。参与该筹商的患者近6000名之多。来自全寰球的行业大家在ASCO现场共同凝听了这项大型临床筹商的进修打算与极佳的阳性成果。
也恰是在一次次曝光中,国外往日对中国翻新药公司过火临床数据质地的彷徨也逐渐隐藏。
早在2015年7月22日,原国度食药监局曾条目张开药物临床进修数据自查核查。在这一“史上最严数据核查条目”下,简略申诉企业主动撤退了申诉材料。该事一度被业内称为“722惨案”。
2016年,澳大利亚记者将前述情况误称为“80%的中国临床数据作秀”,这一表述又被二次援用,极大挫伤了中国在干系领域的国际声誉。尽管而后中国药监机构抓续出台政策,确保国内药企临床进修数据的准确性,但也曾造成的对外印象不会豪恣消失。
在2023年ASCO会议上,百利天恒的双抗ADC(抗体偶联药物) BL-B01D1凭优异的国内临床数据迷惑到一众跨国药企的眼神,但也没躲过在数据可靠性方面的疑虑。
百利天恒董事长朱义告诉界面新闻,收获于这款药的好意思国买方百时好意思施贵宝的充分尽调,国外同业对中国数据的疑虑最终得以撤消。
 图为百利天恒董事长朱义 图片起首:百利天恒
图为百利天恒董事长朱义 图片起首:百利天恒
尽调期间,百时好意思施贵宝派出第三方前去中国的临床进修机构拷贝肿瘤原始影像,再行评估筹商论断;又前去百利天恒在成都的工场和研发中心,核查BL-B01D1工艺发展进程中的逻辑性、数据坚实性。
惟一径直赢得百时好意思施贵宝全权信任的数据来自公司位于好意思国的翻新药研发中心“西雅图免疫”。
这是百利天恒早在2014年就开荒、借好意思国脉土翻重生态作念原始翻新的场合,认真的是BL-B01D1的临床前早期筹商部分。“西雅图免疫提供的数传闻什么他们(百时好意思施贵宝)就认什么,就惟有不了了的场合还要再问问,仅此费力,连那场合都没去。”朱义对界面新闻说。
好在每一处都剿袭住了进修。2023年12月,百利天恒与百时好意思施贵宝对外浮现了的配合音问,BL-B01D1创下84亿好意思元交游总价记录,而后又在同类分子中率先完成公共首个III期临床筹商。
与百时好意思施贵宝达成配合后,两边共同探求对利益干系方的浮现口径,写在第一条的即是“该交游是基于一项超800名患者的大样本量数据”。在朱义看来,这是百时好意思施贵宝对公司研发水和气资产质地的认同。
幸亏走过的“自证”之路并无空费。朱义嗅觉到而后跨国药企们看百利天恒的在研名目数据时,已不再缅想临床进修数据的质地。
算作国内较早开启国际化策略的公司,复宏汉霖也在与跨国药企的配合中渐渐赢得信任。
公司首席商务发展官、高档副总裁曹平回忆,2022年,复宏汉霖与好意思国欧加隆共同创造了一笔生物近似药领域近6年来的最大配合。但其时新冠疫情突袭,欧加隆曾一度担忧复宏汉霖算作中国企业的委用保险,直到公司以高效的扩充力和实践行为已毕了容许。
04 恭候“重磅炸弹”
2025年的前5个月中,在公共首付款大于5000万好意思元界限的商务拓展交游中,中国占比也曾从2021年的5%提高至42%。
 图为中国翻新药岁首交游情况 制图:界面新闻 何苗
图为中国翻新药岁首交游情况 制图:界面新闻 何苗
而当手上的居品更具竞争力,国内翻新药企们也已启动不霸道于只是将新药授权出去。进化成为国际化公司,躬行开发、销售我方的新药成为一些东说念主最终的主见。
只不外无论什么行业,参加每一个新市集要驯顺和相宜当地的监管规章和生意环境。更何况作念出一款翻新药的进程号称冗长,完成这一链条成为任何东说念主都无法独自实现的豪举。
薛彤彤向界面新闻分析,这让如今的中国翻新药公司去找国外配合资伴的确成为一条例必选择,并同期能赢得现款酬谢、打响公司品牌,来实现资产价值。
而对意在构建公共体系的国内翻新药公司来说,现款酬谢以至不是惟一首要的。
百利天恒找配合者时,朱义长期坚抓不作念买断性交游,而要分享BL-B01D1在国外的开发和收益权。公司也直言但愿借与百时好意思施贵宝的配合,促进其建立起在公共的临床开发和生意化智力。
这背后的原因是,神枪手都是靠枪弹喂出来的。而与国外大厂的洽谈和配合就是一次次射击熟识。
贺峰向界面新闻例如,国外跨国药企对居品的条目相当高,在调研评估潜在居品时,它们会有多轮既杂又细的问题。从发现筹商、临床筹商,到工艺坐蓐,每个设施回应的问题加起来有成百上千。而在梳理念念路和回应问题的进程中,中国药企实践上不错了解并学习到国外跨国药企在各个设施的理会、把控与经验。
年青的宜联生物相同如斯成长。初期,其与国内的翻新药公司无为配合,由此赢得利润,也考证时候、蕴蓄数据和竞争力。确立三年后,公司的授权对象则膨胀到在好意思股上市的再鼎医药和BioNtech。
前者让宜联生物第一次拿到了国外的资金——这是国内公司给不了的价钱;后者的无情则帮公司在CMC(化学、制造、搁置)设施和临床筹商中抓续提高 。
在薛彤彤看来,有资金回笼、有配合资伴、有学习进程,中国药企才能逐渐蕴蓄起国际化的体系和经验,在国外鼓励翻新药管线,直到信得过靠我方作念完国际III期临床、递交上市苦求。而再往后,企业又将濒临生意化上的问题,即使这个设施仍将交给配合资伴,但这一进程中,中国药企的分派权无疑将越来越大。
而这么的想象在百利天恒身上已启动体现。
朱义告诉界面新闻,公司有筹商在2025年到2030年这五年造成跨国药企的框架,包括在国表里具备早期研发、临床开发、生意化、坐蓐四方面的智力。
7月2昼夜深,半年没更新一又友圈的朱义接连转发四条动态,内容都是BL-B01D1休养鼻咽癌的III期临床进修在期平分析达到主要止境的音问。这意味着,有筹商中的5年里,百利天恒距离成为跨国药企的主见又进了一步。
对于当今的出海激越,曹平对其的评价为“这是一个令东说念主怡悦的期间”。但她也同期领导,怡悦之余照旧要看后续。
曹平以为,就当今而言,药企间大宗的配合发生在了早期资产上,但翻新药领域具有较强的不细目性——居品后续能否进临床、能否在国外获批上市、能否建立百亿好意思元销售额都是未知。
她以为开云(中国)开云kaiyun·官方网站,惟有当中国公司原研开发的翻新药置身公共“重磅炸弹”行列,才记号着中国翻新药信得过参加一个光辉的期间。